허소윤 , 이경태 , 홍영기
하이드록시프로필 메틸셀룰로스 함량에 따른 의료용 실크 피브로인 나노섬유 제조와 특성
Fabrication and Properties of Silk Fibroin Nanofibrous Sheets with Hydroxypropyl Methylcellulose Content for Biomedical Applications
So Yun Heo, Gyeong Tae Lee, Young Ki Hong
Abstract: Electrospun silk fibroin (SF) nanofibers have emerged as promising materials for primary wound dressings due to their biodegradability, biocompatibility, and high specific surface area. Hydroxypropyl methylcellulose (HPMC), a semi-synthetic hydrophilic polymer, has also been widely utilized in biomedical applications owing to its water absorption capacity and biocompatibility. In this study, SF and HPMC were combined to fabricate SF/ HPMC nanofibrous (SHNFs) via electrospinning, and the effects of HPMC content on their physicochemical and biological properties were systematically evaluated. As the HPMC concentration increased, the viscosity of the spinning solution rose nonlinearly while its electrical conductivity decreased, adversely affecting process stability. Above 1.5% HPMC, fiber morphology became increasingly non-uniform, and the basis weight significantly declined. SHNF1 exhibited the highest tensile strength (3.01 MPa), but no consistent trend was observed with increasing HPMC content. Although fiber uniformity and mat density decreased, the water absorption capacity improved progressively with HPMC addition, suggesting a dominant role of HPMC’s inherent hydrophilicity. FTIR spectra showed a shift in the Amide I band between RSF and SHNFs, implying a change in molecular environment, while no clear secondary structural transitions were detected among SHNF samples. Cytotoxicity assessment using LDH assay revealed no significant differences from the low control group, confirming minimal cytotoxic effects on NIH 3T3 fibroblasts. These findings indicate that SHNFs exhibit excellent hydrophilicity and biocompatibility, supporting their potential use as effective primary wound dressings. Based on these findings, the optimal HPMC concentration was determined to be 1% (w/v), balancing spinnability, structural integrity, and functional performance.
Keywords: wound dressing , absorption , electrospinning , silk fibroin , HPMC
1. 서 론
피부는 표피, 진피, 피하지방 총 세 부분으로 이루어져 있다. 표피는 각질세포를 포함하는 얇은 층으로 구성되고 이때 생성된 각질세포는 피부를 보호한다. 진피는 표피 아래에 있는 두꺼운 층으로 외부에서 발생하는 압력과 장력으로부터 신체를 보호하며, 다양한 세포 및 ECM(extracellular matrix)을 포함한다[1]. 피부 손상은 체내 환경의 안정성과 정상적인 생리 기능이 방해를 받아 감염, 체액 손실 및 체온 조절 장애와 같은 위험을 초래할 수 있다[2]. 효율적인 상처 치료를 위해 고분자 및 복합 재료로 의료용 창상 피복재 개발이 활발히 이루어지고 있다. 이는 상처 회복에 중요한 세포의 이동, 접착, 분화 및 증식 단계를 수행하기 위한 유리한 환경을 제공하여 상처 치료를 가속할 수 있다[3].
의료용 창상 피복재는 상처 치유와 피부 조직 재생을 촉진하는 데 중요한 역할을 한다. 이상적인 의료용 창상 피복재는 과도한 삼출물은 흡수하되 상처를 습윤 상태로 유지시키며, 상처를 보호하고, 기체 및 수분 교환이 원활한 투과성을 지녀야 한다. 상처에 자극 없이 쉽게 제거할 수 있어야 하고, 항균 작용을 제공해야 한다. 또한, 무독성, 비알레르기성, 비감작성, 세포부착성과 같은 생체적합성을 가지며, 멸균 처리되어야 한다.
실크는 누에 고치에서 얻어지는 자연 단백질 섬유로, 크게 두 가지 단백질인 세리신과 피브로인으로 구성되어 있다. 세리신은 고치를 감싸는 접착제 역할을 하며, 피브로인은 섬유의 구조적 강도를 제공한다. 미국 FDA는 실크 피브로인(silk fibroin, SF)을 의료용 소재로 승인하였으며, 이는 그 안전성과 효능이 입증되었음을 의미한다. SF는 뛰어난 생체적합성, 생분해성, 그리고 기계적 물성을 바탕으로 다양한 형태의 의료용 창상 피복재 소재로 개발되어 왔으며, 세포의 증식, 이동 및 분화를 유도하여 조직 재생을 향상시키고 상처 치유를 촉진하는 데 활용되고 있다[4]. 하지만 SF 단독으로 제조된 소재는 여러 물성적 한계를 가지며, 이를 극복하기 위한 복합소재 개발과 제조 공정의 고도화가 최근 연구의 주요 방향으로 자리 잡고 있다. SF 필름은 높은 결정성으로 인해 유연성이 제한되는 단점이 보고되었으며, 이를 보완하기 위해 PVA(polyvinyl alcohol)와의 복합화를 통해 물리적 특성을 향상시킨 연구가 진행된 바 있다[5]. 또한, SF는 본래 항균성이 부족하여 이를 극복하기 위해 키토산, 은 나노입자, 커큐민 등의 생리활성 물질과의 복합화가 시도되고 있다[6]. 이와 같은 연구들은 SF의 본래 특성을 유지하면서 단점을 보완하고, 고기능성의 상처 치료 소재로서의 적용 가능성을 넓히고자 하는 다양한 방향성을 제시한다.
SF 나노섬유는 높은 비표면적과 우수한 생체적합성, 기계적 특성으로 이상적인 의료용 창상 피복재의 특성인 흡수력, 상처 보호, 투과성, 생체적합성 특성을 지니고 있다. SF 나노섬유를 제작하는 방법 중 하나인 전기방사법는 고분자 용액과 드럼형 수집체 사이의 전위차에 의해 나노섬유를 만드는 공정으로 전기방사 공정에서 고분자 용액의 물성은 생성되는 나노섬유의 구조적 특성에 영향을 미친다[7]. 용액의 전기전도도가 높을수록 전하 이동이 용이해져 섬유의 직경이 감소하고 균일도가 향상되는 경향이 있다. 저점도 용액 방사 시 비드(Bead)가 형성될 수 있고, 고점도 용액 방사 시 섬유의 생성을 방해하고, 마이크로섬유를 생성할 수 있다. 이러한 변수들은 결과적으로 섬유의 형태, 직경, 기공률, 다공성 등 미세구조 특성에 영향을 주며, 세포 부착, 영양분 교환 등 조직 공학적 응용에서 매우 중요한 요소로 작용한다[8]. 방사 용액의 물성을 정밀하게 제어함으로써, 전기방사 기술은 다양한 천연 및 합성 고분자를 활용하여 조직 공학 및 재생 의학에 적합한 물리적, 화학적, 생물학적, 열적 및 기계적 특성을 지닌 나노구조 생체 재료를 제조할 수 있는 유망한 방법으로 주목받고 있다. 특히, 전기방사로 제조된 나노섬유는 높은 표면적과 다공성, 상호 연결된 기공 구조를 갖추고 있어 세포 부착과 성장을 유도하고, ECM을 모방할 수 있는 발판으로서 적합하다[9].
하이드록시프로필 메틸셀룰로스(HPMC)는 천연 고분자인 셀룰로스를 화학적으로 변형하여 제조한 반합성 중합체이다. HPMC는 수용성 셀룰로스로 친수성, 비독성, 생분해성, 생체적합성, 식용성 및 기계적 특성을 가지고 있어 생체 조직 공학 재료로 사용할 수 있다. 또한, HPMC는 농도에 따라 점도가 비선형적으로 증가하는 특성을 가지며, 이는 약물 방출 제어나 필름 제형의 가공성 조절에 유용하게 활용된다[10]. 섬유나 필름에 적용될 경우 우수한 수분 흡수 능력을 발휘하는 것으로 보고되고 있다[11].
본 연구에서는 재생성 실크 피브로인(RSF)과 셀룰로스 유도체인 HPMC를 혼합하여 전기방사 방식으로 나노섬유를 제조하고, HPMC 함량 변화에 따른 방사성, 수율, 형태학적, 화학적, 기계적 및 생물학적 특성 등을 종합적으로 분석하였다. 이를 통해 의료용 창상 피복재에 최적화된 SF/HPMC nanofibrous (SHNFs)의 제조 조건과 물성을 규명하고자 한다.
2. 실험 및 방법
2.1. 재 료
SF은 Bombyx mori 누에 고치에서 추출되었다. SF 수용액 제조 시 사용된 sodium carbonate anhydrous [TeX:] $$\left(\mathrm{Na}_2 \mathrm{CO}_3\right),$$ calcium chloride anhydrous [TeX:] $$\left(\mathrm{CaCl}_2\right)$$와 ethyl alcohol (EtOH, 99.9%)는 Duksan에서 구매하였으며, 투석 과정 시 사용된 Dialysis Cellulose Tubing (MWCO 12400, 99.9% retention)은 Sigma-Aldrich에서 구매하였다. (Hydroxypropyl)methyl cellulose (Mn ~86,000)은 Sigma-Aldrich에서, SHNFs 수용액 제조 시 용매로 사용된 formic acid (99.9%)는 Samchun에서 구매하여 사용하였다.
2.2. SF 수용액 제조
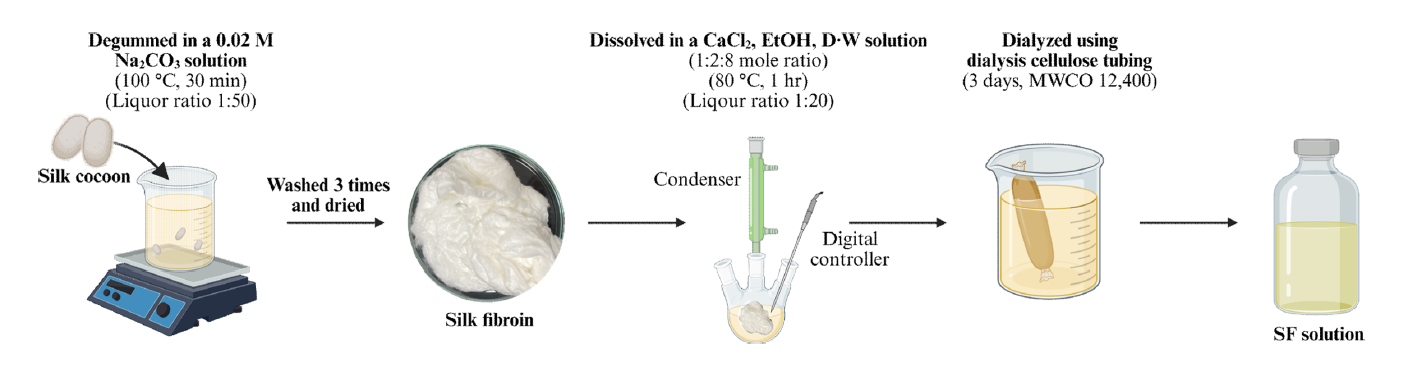
SF 수용액은 Figure 1과 같이 제조하였다. 흙과 이물질이 제거된 Bombyx mori의 누에 고치를 0.02 M [TeX:] $$\left(\mathrm{Na}_2 \mathrm{CO}_3\right),$$ 용액에서 [TeX:] $$100^{\circ} \mathrm{C},$$ 30 min 간 탈검 과정을 거쳐 세리신을 제거한 후, 증류수로 3 회 세척하고 건조하였다. 건조된 SF는 3원 용매법[TeX:] $$\left(\mathrm{CaCl}_2 / \mathrm{EtOH} / \mathrm{D} \cdot \mathrm{W}\right)$$을 이용하여 5% (w/v)로 용해시켰다. 용해된 용액은 3일간 dialysis cellulose tubing (MWCO 12,400)을 이용하여 deionized water (D·W)에서 투석을 진행하였고, D·W는 하루에 한 번 교체하여 용액에 잔류하는 혼합용액과 저분자량 SF를 여과한 후, SF 수용액을 제조하였다.
2.3. 전기방사법을 이용한 SHNFs 제조
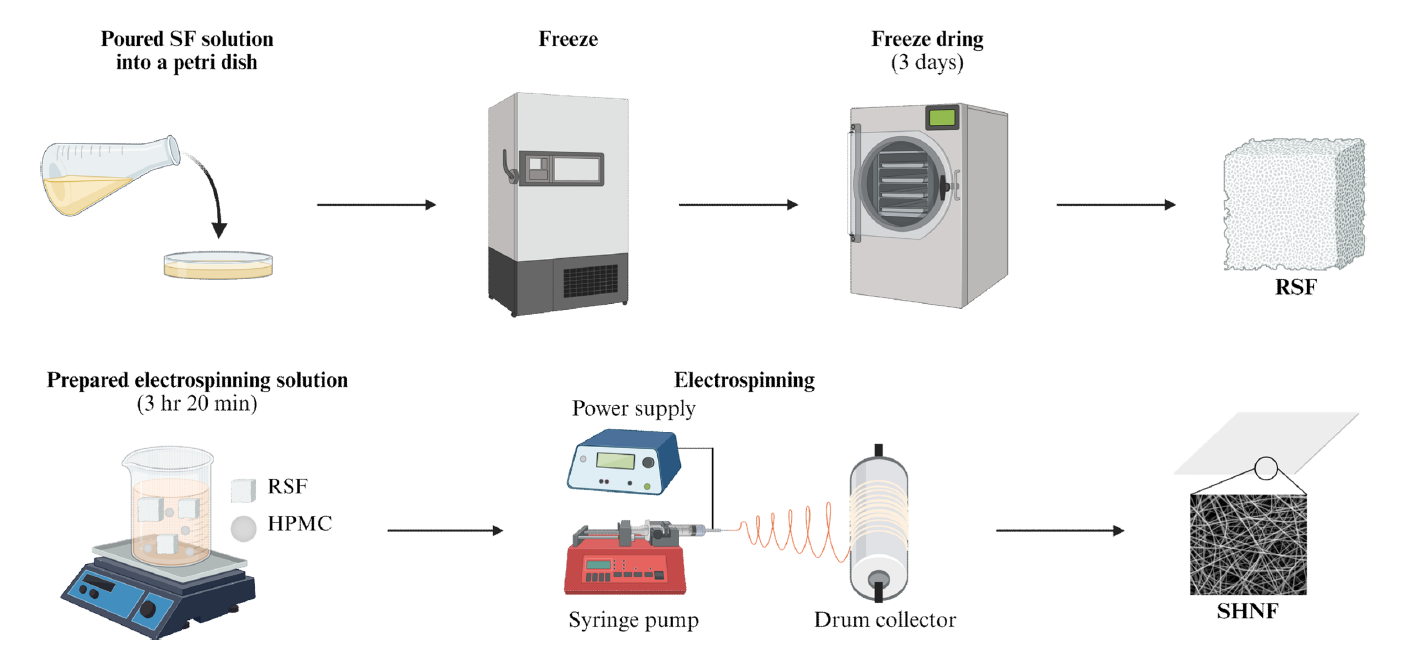
방사 용액의 제조 및 전기방사를 통한 나노섬유 형성 과정은 Figure 2에 나타내었다. SF 수용액을 [TeX:] $$-50^{\circ} \mathrm{C}$$에서 3일간 동결 건조하여 얻어진 RSF는 [TeX:] $$40^{\circ} \mathrm{C}$$ 오븐에서 보관하였다. RSF는 12% (w/v)로 고정하고[12], HPMC는 0%부터 5%(w/v)까지 함량을 달리하여 formic acid (FA)에 용해시켜 SHNFs 수용액을 제조하였으며, Table 1에 조성을 나타내었다. HPMC의 농도에 따라 SHNFs 이름의 마지막 숫자를 달리하여 명명하였다. HPMC 함량에 따른 섬유의 형상을 확인하기 위해 다양한 비율로 혼합하였다. SHNFs 수용액은 21 G 바늘을 통해 양전압 13 kV, 음전압 1.5 kV, 유량 0.800ml/h로 전기방사(NanoNC, Seoul , Korea)하였다. 드럼형 수집체의 회전 속도는 150 rpm, 바늘과 수집체 사이 거리는 10 cm로 유지하였다.
Table 1.
| RSF (%) | FA (ml) | HPMC (%) | |
|---|---|---|---|
| SHNF0 | 12 | 20 | 0 |
| SHNF0.5 | 12 | 20 | 0.5 |
| SHNF1 | 12 | 20 | 1 |
| SHNF1.5 | 12 | 20 | 1.5 |
| SHNF2 | 12 | 20 | 2 |
| SHNF3 | 12 | 20 | 3 |
| SHNF4 | 12 | 20 | 4 |
2.4. SHNFs 수용액 물성
SHNFs 수용액의 전기전도도 측정: SHNFs 수용액의 전기 방사 적합성을 평가하기 위해, Istek사의 EC-400L 전도도 측정기를 사용하여 [TeX:] $$25^{\circ} \mathrm{C}$$에서 전기전도도를 측정하였다. 측정 시, 전도도 셀을 용액에 침지하여 측정하였으며, 전기전도도 값은 용액의 전기방사 특성 및 전기방사 공정에 미치는 영향을 분석하는 데 활용되었다.
SHNFs 수용액의 점도 측정: 전기방사 공정에서의 거동을 평가하기 위해, SHNFs 수용액을 회전 레오미터(Rotational rheometer)인 Anton Paar MCR 102를 사용하여 점도를 측정하였다. [TeX:] $$25^{\circ} \mathrm{C}$$에서 진행되었으며, 총 120초 동안 6초 간격으로 점도를 측정하였다. 측정된 점도 값은 용액의 유동 특성과 전기방사 공정에 미치는 영향을 분석하는 데 활용되었다.
2.5. 평량 측정
HPMC 함량에 따른 방사 공정의 영향을 평가하기 위해, KS K ISO 9073-1:2018(비직물의 시험 방법 - 제1부: 단위 면적당 질량의 측정) 규격에 따라 SHNFs의 평량을 산출하였다. 각 조건별로 5회 반복 측정하여 평균값을 도출하였으며, HPMC 농도 변화가 섬유 형성 효율성과 방사 안정성에 미치는 영향을 정량적으로 분석하였다.
2.6. 형태학적 특성 평가
SHNFs의 형태학적 특성 분석을 위해 전계방사형 주사전자현미경(Field Emission Scanning Electron Microscope, FESEM; Apreo 2, Thermo Fisher Scientific, USA)을 사용하였다. 분석에 앞서, 시료 표면에 약 10.66 nm 두께의 백금 (Pt) 코팅을 실시하였다. 관찰은 가속 전압 5 kV 조건에서 수행하였으며, 500배에서 50,000배까지 다양한 배율로 image를 획득하였고, 결과 분석에는 50,000배 image를 사용하였다. Image J 소프트웨어(Version 1.54, National Institutes of Health, USA)를 이용하여 섬유 직경을 분석하였으며, 각 시료에서 총 70개의 섬유 직경을 측정하여 정량 분석에 사용하였다.
2.7. 화학적 특성 평가
SHNFs의 화학적 구조를 분석하기 위해 Jasco사의 FT/IR-4X 적외선 분광기를 사용하여 ATR (attenuated total reflectance) 모드로 FTIR (Fourier transform infrared) spectra을 측정하였다. [TeX:] $$4 \mathrm{~cm}^{-1}$$의 분해능으로 [TeX:] $$4000 \mathrm{~cm}^{-1}$$에서 [TeX:] $$650 \mathrm{~cm}^{-1}$$까지의 파수 범위에서 수행되었으며, 각 spectra은 32회 스캔한 평균으로 얻어졌다.
2.8. 기계적 특성 평가
HPMC의 함량에 따라 제조된 SHNFs의 기계적 특성 평가는 universal testing machine (UTM, AGS-X STD, Shimadzu)을 사용하여 수행되었다. ASTM D882-21 (Standard Test Method for Tensile Properties of Thin Plastic Sheeting, 개정 2021) 규격을 적용하여, 기계 방향(machine direction, MD)으로 길이 150 mm, 너비 25 mm의 스트립 형태로 절단하였으며 5회 측정을 진행하였다. 파지 거리 50 mm, 인장 속도 50 mm/min 조건으로 수행하였다.
2.9. 흡수율 시험
SHNFs의 흡수율 측정은 ISO 20158:2018 (섬유제품 - 흡수 시간 및 흡수 용량의 측정) 규격에 기반하여 수행하였다. 시료는 면적 100 cm2 (10 cm×10 cm) 크기로 제단하여 건조 후 무게를 측정하였으며, 이후 증류수에 일정 시간 동안 침지하였다. 각 조건별로 5회 반복 측정하여 평균 흡수율을 도출하였으며, 흡수율은 다음 식 (1)에 따라 계산하였다:
[TeX:] $$W_f$$=흡수 후 무게
[TeX:] $$W_i$$=흡수 전 무게
2.10. In vitro 세포독성 평가
SHNFs의 세포독성 평가는 KS ISO 10993-5 (의료기기의 생물학적 평가 - 제5부: 세포독성 시험) 기준에 따라 LDH assay를 통해 수행하였다. NIH 3T3 섬유아세포는 10% 우태아혈청(FBS)과 1% penicillin-streptomycin이 첨가된 Dulbecco’s modified eagle medium (DMEM)에서 [TeX:] $$37^{\circ} \mathrm{C}$$, 5% [TeX:] $$\mathrm{CO}_2$$ 조건에서 배양하였다. 제조된 SHNFs는 자외선(UV) 조사를 이용하여 양면 각각 15분씩, 총 30분간 멸균하였으며, 용출 조건은 KS ISO 10993-12 기준에 따라 DMEM에 24시간 침적하여 SHNFs extract를 제조하였다. 이후 96-well plate에 100% extract (100%_E), 50% extract (50%_E)를 각각 100 μl씩 처리하여 세포를 처리하였다. 배양 후 상층액을 회수하여 LDH 분석 키트로 제조사 지침에 따라 분석하였으며, ELISA를 이용해 450 nm에서 흡광도를 측정하였다. 각 시료의 흡광도를 low control 군의 평균 흡광도로 정규화하였으며, 아래의 식 (2)를 이용하여 상대적인 LDH 방출량을 산출하였다.
3. 결과 및 고찰
3.1. SHNFs 수용액 물성 분석
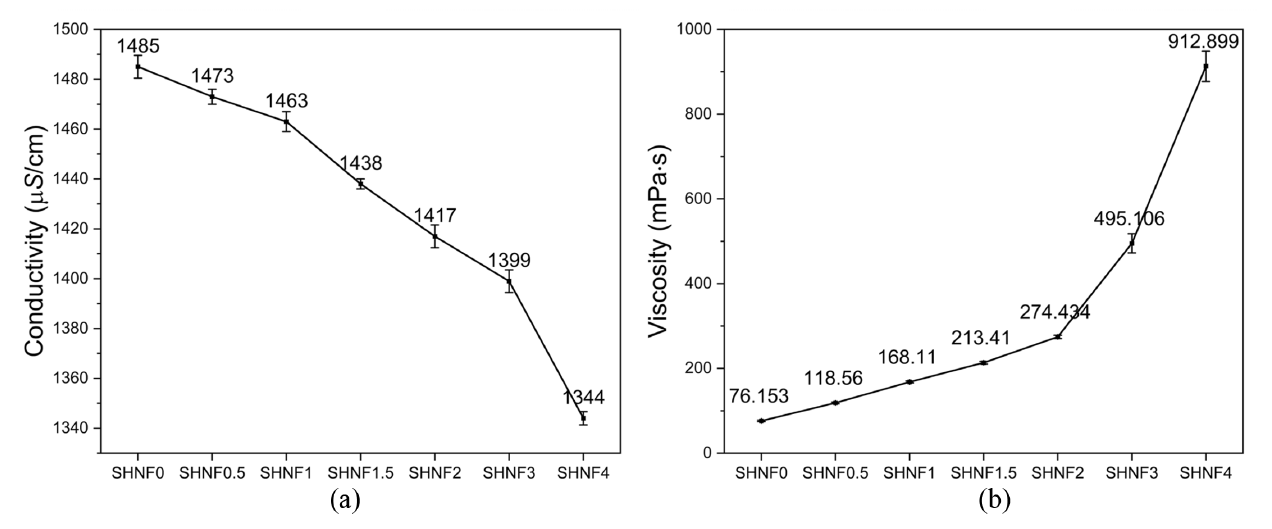
HPMC 함량에 따른 SHNFs 수용액의 물성을 평가하기 위해 진행된 전기전도도 및 점도 분석을 Figure 3(a)와 Figure 3(b)에 나타내었으며, 평균±표준편차(mean±SD)로 표현하였다. HPMC의 첨가량이 SHNFs 수용액의 물성에 미치는 영향을 분석한 결과, HPMC의 농도가 0%에서 4%로 증가함에 따라 전기전도도 분석 결과는 1485 μS/cm에서 1344 μS/cm로 감소하였다. 점도 분석 결과는 76.153 mPa·s에서 912.899 mPa·s로 약 12배 증가하였다. 이러한 경향은 비이온성 고분자인 HPMC가 FA에 용해되어 점도를 증가시키고, 이온의 이동을 방해하여 전기전도도는 감소하는 경향을 나타내었다고 판단된다[13]. 결과적으로, HPMC는 점도를 제어하고 전기전도도에 영향을 미치는 중요한 조성 인자이며, 이는 이후 전기방사 공정의 안정성과 섬유 형성 특성에 직결되는 중요한 요소로 작용할 수 있다.
Figure 3.
3.2. SHNFs의 평량 측정 분석
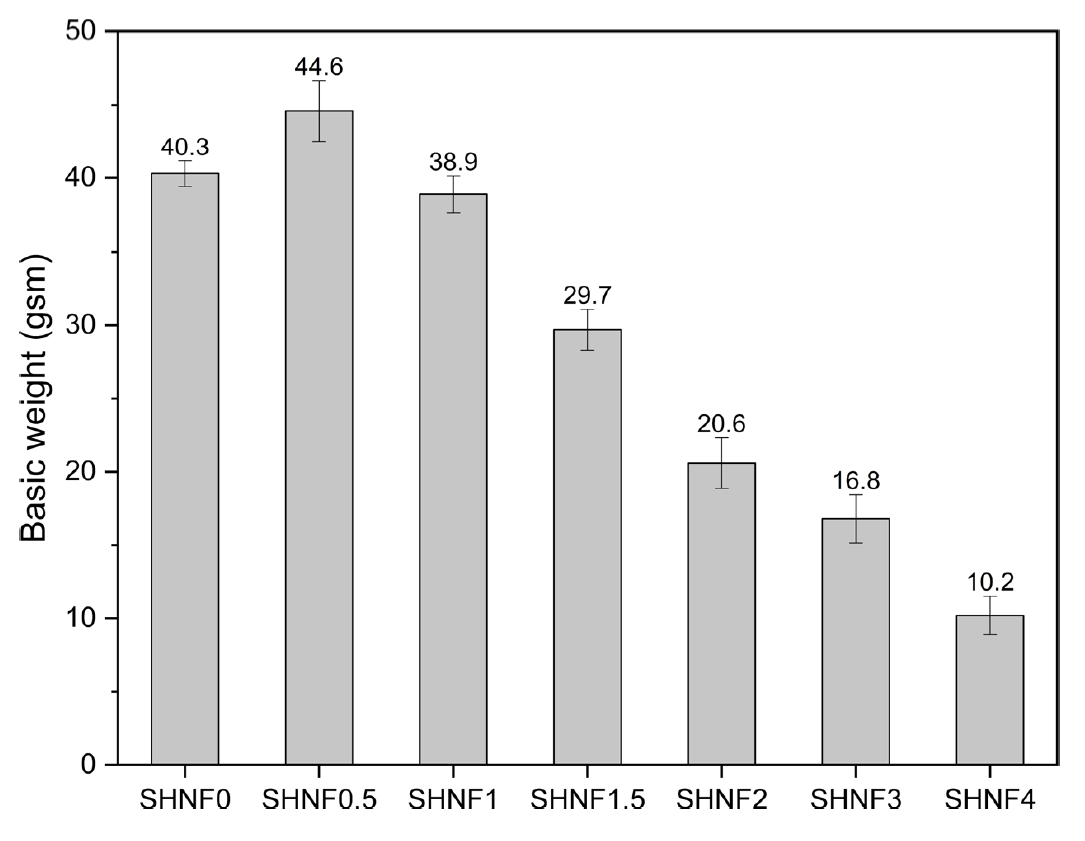
HPMC 함량 변화에 따른 SHNFs의 형성 정도를 정량적으로 평가하기 위하여 Figure 4에 평량 측정 결과를 나타내었다. SHNF0.5는 44.6 gsm으로 가장 높은 평량을 보였으며, HPMC 농도가 1% 이상으로 증가함에 SHNF0과 비교하여 평량은 감소하는 것을 확인하였다. HPMC의 농도 증가에 따라 전기전도도의 감소와 점도의 증가로 용액 내 이온의 이동이 제한되고, 일정 농도 이상에서는 반고체 구조가 형성되어 전기방사 공정의 연속성과 섬유 형성 효율을 저해한 것으로 판단된다[14]. 평량의 감소는 섬유의 밀집도 및 두께의 저하를 의미하며, 창상 피복재의 주요 기능인 상처 부위 보호, 감염 차단, 외부 자극 완충 능력에 영향을 미칠 수 있다.
3.3. SHNFs의 형태학적 특성 분석
HPMC 함량 변화에 따른 SHNFs의 형태학적 변화를 평가하기 위하여 Figure 5에 SEM image를 나타내었다. 섬유 직경 분석 결과, SHNF0은 146.16±45.61 nm, SHNF0.5는 253.36±49.50 nm, SHNF1 193.07±36.74 nm, SHNF1.5는 206.59±53.27 nm, SHNF2는 274.54±122.44 nm, SHNF3는 370.43±123.67 nm, SHNF4는 376.52±146.56 nm로 확인되었다. 방사 용액의 전기전도도가 증가하면 용액 내 전하 밀도가 증가하여, 전기장에 의해 생성된 jet이 더 강한 인장력을 받게 된다[15]. 이는 jet의 연신성가 향상되어 직경 감소와 균일한 섬유 형성이 유도된다. 점도는 전기방사 공정에서 섬유 형성에 중요한 영향을 미치는 인자로, 적정 수준의 점도에서는 용액 내 고분자 사슬 간의 얽힘이 안정적으로 발생하여 jet의 연속성과 인장성이 유지되어 섬유 직경이 감소하고 균일한 섬유가 형성되는 경향이 있다[16]. 그러나 점도가 너무 낮으면 jet 형성이 불안정해져 비드가 발생하고, 반대로 점도가 과도하게 높을 경우 용액의 유동성이 저하되어 전기장이 jet를 충분히 인장하지 못하게 되며, 이로 인해 섬유 직경이 증가하거나 방사 자체가 어려워질 수 있다[17]. SHNF0에서는 전기전도도는 높으나 낮은 점도로 불균일한 섬유와 비드가 형성이 확인되었으며, SHNF0.5, 1에서는 섬유의 균일함이 관찰되었다. HPMC 함량이 1.5% 이상에서는 거미줄처럼 얇고 불균일한 섬유가 관찰되었으며, 이는 과도한 점도로 인해 전기방사 중 jet 형성이 불안정해지고, 고분자가 분무되거나 섬유가 끊어지면서 생성된 것으로 판단된다. SHNF4는 섬유의 연속적인 형성이 확인되지 않아 섬유 구조의 확보가 어려운 것으로 나타나[18], 이후의 섬유특성 평가 및 세포독성 분석에서 제외하였다.
Figure 5.

3.4. SHNFs의 화학적 특성 분석
HPMC 함량에 따른 SHNFs의 화학적 구조를 특성화하기 위해 ATR-FTIR 분석을 Figure 6에 제시하였다. Figure 6(a)에는 HPMC, RSF, FA, SHNF1를 나타내었으며, Figure 6(b)는 제조된 SHNFs의 spectra를 나타내었다. 또한, 비교분석을 위해 Figure 6(c)에서 SF의 주요 peak와 Figure 6(d)에서 HPMC 함량에 따른 분석을 중점적으로 진행하였다.
FA의 FTIR 측정 결과, [TeX:] $$3057 \mathrm{~cm}^{-1}$$ (O-H stretching), [TeX:] $$1687 \mathrm{~cm}^{-1}$$ (C=O stretching), [TeX:] $$1352 \mathrm{~cm}^{-1}$$ (O-H bending), [TeX:] $$1163 \mathrm{~cm}^{-1}$$ (C-O stretching), [TeX:] $$1063 \mathrm{~cm}^{-1}$$ (C-O stretching), [TeX:] $$816 \mathrm{~cm}^{-1}$$ (C-H bending) peak가 관찰되었다[19]. SHNFs에서 RSF에선 확인되지 않았던 [TeX:] $$1167-1169 \mathrm{~cm}^{-1}$$ 부근의 peak가 새롭게 관찰되었으며, 이는 FA의 C-O stretching ([TeX:] $$1163 \mathrm{~cm}^{-1}$$) 진동과 유사하여 섬유 내 잔류 FA의 영향일 가능성이 있다. 그러나 주요 FA 특성 peak(3057, 1687, 1352, 1063, 816 [TeX:] $$\mathrm{cm}^{-1}$$)가 SHNFs spectra에서 소실된 점과, Figure 6(c)에서 나타낸 모든 SHNFs에서 일정한 세기의 peak인 것을 고려하면, RSF 또는 RSFHPMC 간 새로운 수소결합 구조 형성에 따른 C-O 진동일 가능성도 배제할 수 없다.
Figure 6.
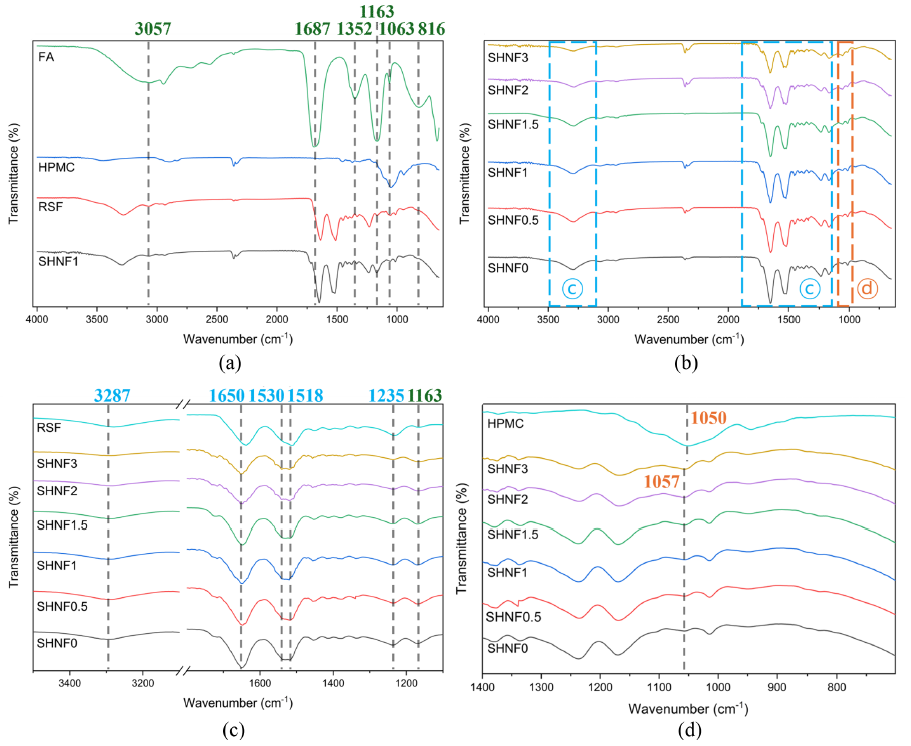
SF는 분자 내 Amide bond에 기인하여 Amide I, II, III 밴드에 해당하는 특성적인 흡수 peak를 나타낸다[20]. RSF에서 [TeX:] $$1638 \mathrm{~cm}^{-1}$$의 Amide I 밴드 (C=O stretching), [TeX:] $$1512 \mathrm{~cm}^{-1}$$의 Amide II 밴드 (N-H bending), [TeX:] $$1232 \mathrm{~cm}^{-1}$$에서의 Amide III 밴드 (C-N stretching)과 [TeX:] $$3280 \mathrm{~cm}^{-1}$$의 N-H stretching의 peak를 관찰하였다. 이는 β-sheet 구조에 해당하는 파수 범위로, RSF가 비교적 높은 결정성을 유지하고 있음을 나타낸다. 제조된 SHNFs에서 [TeX:] $$1650 \mathrm{~cm}^{-1}$$의 Amide I 밴드, [TeX:] $$1530 \mathrm{~cm}^{-1}$$, [TeX:] $$1518 \mathrm{~cm}^{-1}$$의 Amide II 밴드, [TeX:] $$1235 \mathrm{~cm}^{-1}$$에서의 Amide III 밴드와 [TeX:] $$3287 \mathrm{~cm}^{-1}$$의 N-H stretching peak를 관찰하였다. 이러한 변화는 β-sheet 구조가 부분적으로 손상되고, 비정질 구조인 random coil 또는 Silk I 형태로의 전이가 발생하여 전반적으로 파수가 증가함을 시사한다. 이는 FA에 의한 용해 과정에서 수소결합이 붕괴되고, 전기방사 중 급격한 용매 증발로 인해 폴리펩타이드 사슬이 재배열될 시간 없이 고정되었기 때문으로 판단된다[21].
HPMC 함량에 따른 SHNFs의 FTIR spectra을 Figure 6(d)에 나타내었다. HPMC에서는 [TeX:] $$1050 \mathrm{~cm}^{-1}$$에서 C-O stretching 진동에 해당하는 특성 peak가 확인되었으나[22], HPMC가 첨가되지 않은 SHNF0에서는 해당 peak가 관찰되지 않았다. SHNF0.5, 1, 1.5, 2, 3은 peak가 [TeX:] $$1057 \mathrm{~cm}^{-1}$$로 shift되었고, 이는 HPMC의 C-O 그룹이 SF의 -OH와 전하 분포 재편성이나 입체 구조 변화로 인해 결합 강도가 증가하여 blue shift가 발생한 것으로 판단된다[23].
3.5. SHNFs의 기계적 특성 분석
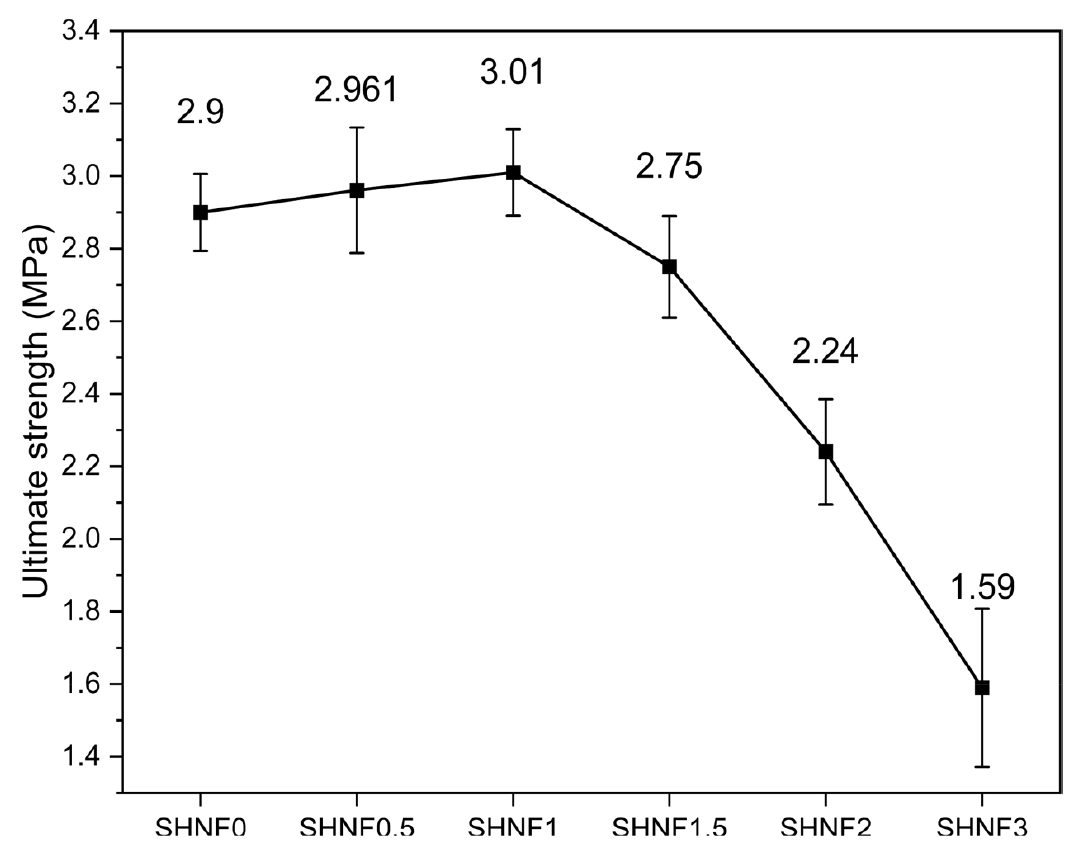
HPMC 함량에 따른 SHNFs의 기계적 특성을 평가하기 위해 인장강도 시험을 실시하였으며, 그 결과를 Figure 7에 제시하였다. SHNF0의 인장강도는 2.90 MPa였으며, SHNF0.5부터 SHNF3까지 각각 2.96 MPa, 3.01 MPa, 2.75 MPa, 2.24 MPa, 1.59 MPa로 나타났다. 적정량의 HPMC 첨가는 섬유 직경 감소를 유도하여 기계적 강도 향상에 기여했으나, 과량 첨가는 섬유 직경 증가 및 불균일성을 초래해 강도를 약화시켰다. HPMC 함량이 1.5% 이상으로 증가함에 따라 인장강도는 감소하는 경향이 나타났으며, 이는 섬유 직경 증가 외에도 섬유의 연속성과 균일성 저하, 전반적인 섬유 밀집도 및 두께(평량) 감소의 영향으로 판단된다. 특히 SHNF1.5와 SHNF2는 상대적으로 섬유 직경이 감소한 시료임에도 불구하고 인장강도가 SHNF0보다 낮게 나타났다. 이는 직경의 감소 및 증가만으로 기계적 성능을 설명하기 어려우며, 섬유의 불균일성, 배열, 밀집도, 두께 등 복합적 요인이 기계적 성질에 영향을 미쳤음을 시사한다. 본 연구에서 제조된 SHNFs는 피부 조직의 인장강도 범위(1-32 MPa) 내에 포함되어 생체조직과 유사한 기계적 거동을 나타내었으며, 1차 창상 피복재로서 요구되는 기계적 성질과 기준에 부합하는 특성을 갖춘 것으로 판단된다[24].
3.6. SHNFs의 흡수율 시험 분석
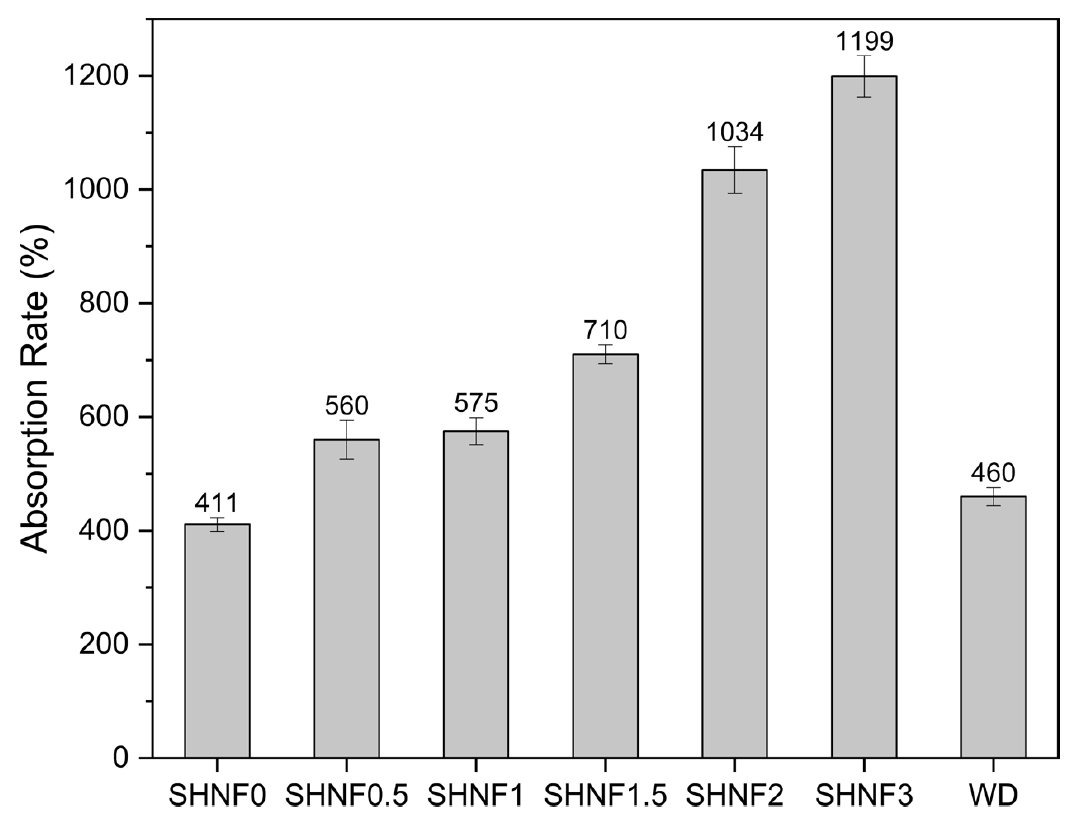
HPMC 함량 변화에 따른 SHNFs의 흡수율(absorption rate, %)을 Figure 8에 나타냈다. SHNF0은 441%의 흡수율을 보였으며, HPMC 함량이 증가함에 따라 흡수율도 증가하여 SHNF0.5는 560%, SHNF1은 575%, SHNF1.5는 710%, SHNF2는 1034%, SHNF3은 1199%의 흡수율을 나타냈다. HPMC 함량이 증가할수록 SHNFs의 평량이 감소하고 섬유의 균일성은 오히려 저하되었음에도 불구하고 흡수율이 상승한 것은 HPMC가 수분을 효과적으로 흡수하고 보유할 수 있는 친수성 고분자임을 뒷받침하며, 단위 중량당 흡수율이 향상되었음을 의미한다. 그 자체의 흡수 능력이 섬유 구조의 밀도나 균일성보다 수분 흡수 성능에 더 큰 영향을 미쳤음을 보여준다. 높은 흡수율은 상처 환경을 습윤하게 만들어주어 조직 재생을 촉진해 빠른 회복과 더불어 통증, 흉터 크기를 감소시킨다. 국내 시판중인 K사의 습윤 피복재(wet dressing, WD) 제품(두께 0.37 mm) 흡수율 결과, 해당 제품은 460%의 흡수율을 보였다. HPMC는 친수성 고분자로서 수분을 효과적으로 흡수하고 보유하는 능력을 갖추고 있어 SHNFs의 의료용 창상 피복재의 상용화 가능성을 보여준다.
3.7. SHNFs의 세포독성 분석
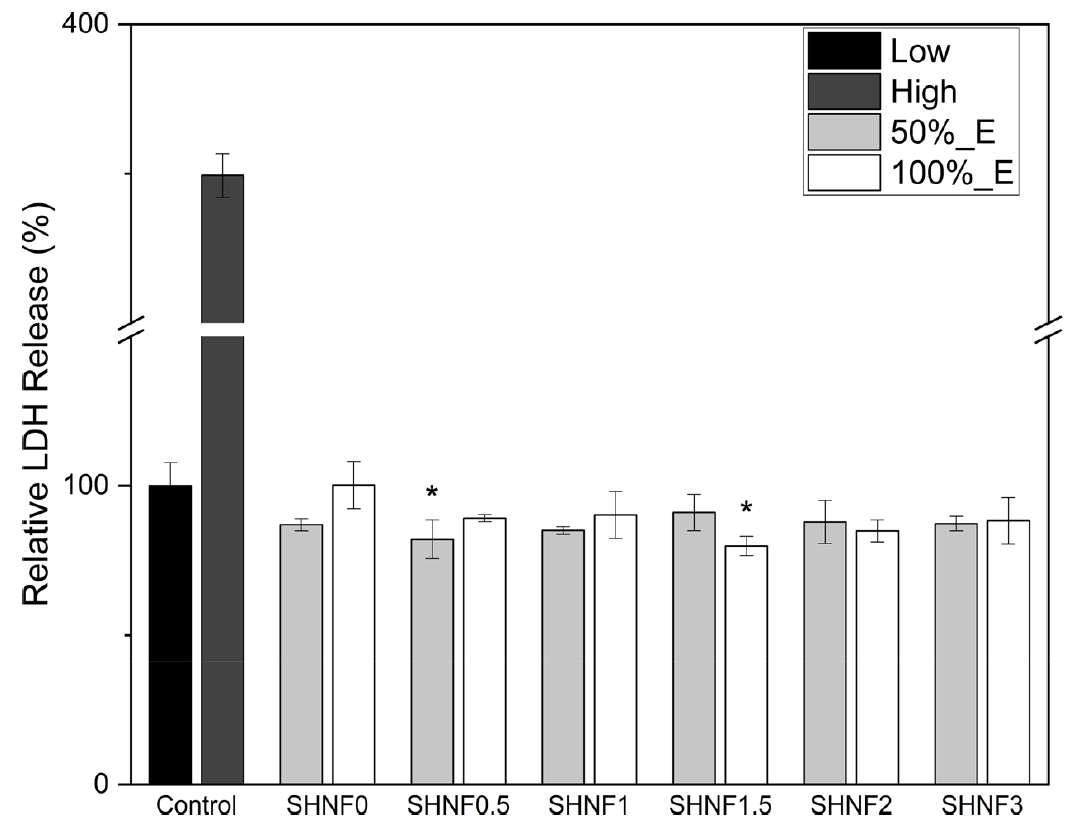
세포독성은 LDH 방출 분석을 통해 평가되었으며, 결과는 Figure 9에 나타내었다. Low control은 자발적 세포사, high control은 완전한 세포막 손상의 기준으로 설정되었으며, low control의 LDH 방출을 100%으로 기준하여 나타내었다. SHNFs는 100%_E 및 50%_E 조건 모두에서 high control에 비해 낮은 LDH 방출을 보였으며, low control과 유사한 수준을 유지하였다. 100%_E 조건에서 SHNF0, SHNF0.5, SHNF1, SHNF1.5, SHNF2, SHNF3는 각각 100.3%, 89.1%, 90.2%, 79.9%, 84.9%, 88.3%의 LDH 방출을 나타냈고, 50%_E 조건에서는 86.9%, 82.1%, 85.0%, 91.0%, 87.9%, 87.3%로 확인되었다. 통계 분석 결과, SHNF0.5 (50%_E) 및 SHNF1.5 (100%_E) 시료는 low control과 비교했을 때 통계적으로 유의하게 낮은 LDH 방출을 나타내었으며(p < 0.05, unpaired t-test), 그 외 시료에서는 유의한 차이가 관찰되지 않았다. 이는 SHNFs가 NIH 3T3 세포에 대해 유의미한 수준의 세포독성을 유발하지 않았음을 시사하며, 모든 시료에서 LDH 방출 수준이 low control과 유사한 범위를 유지하였다.
4. 결 론
본 연구에서는 전기방사법을 이용한 SHNFs 제조 및 특성 평가 결과 다음과 같은 결론을 얻을 수 있었다.
1. HPMC의 함량을 변수로 하여 SHNFs를 제조하는 데 있어 HPMC 함량의 증가는 전기전도도를 감소시키며, 점도는 증가시키는 경향이 확인되었다. 과량의 HPMC 첨가는 전기방사 공정의 연속성과 안정성을 저하시켰다.
2.평량 분석에서는 SHNF1.5부터 수율 저하가 관찰되었다. 형태학적 분석 결과, SHNF1.5부터 섬유의 불균일성이 발생하였으며, SHNF4에서는 연속적 섬유 형성이 이루어지지 않았다.
3.기계적 특성 분석 결과, 제조된 SHNFs는 피부 조직의 인장강도 범위 내에 포함되어 있어, 생체 조직과 유사한 기계적 거동을 보였다. SHNF1은 3.01 MPa로 가장 높은 인장강도를 나타냈으나, 그 이상 농도에서는 더 얇은 섬유 직경에도 불구하고 강도가 오히려 감소하였다. 이는 기계적 성능이 단순한 직경 변화와 차이보다 섬유의 구조적 균일성과 평량 저하 등 복합적인 요인의 영향을 받음을 나타냈다.
4.흡수율 특성 평가를 통하여 HPMC 함량 증가에 따라 지속적으로 상승하였으며, SHNF3는 SHNF0 대비 약 3 배 향상된 수분 흡수력(1199%)을 보였다. 이는 섬유 밀도나 구조적 균일성과 무관하게 HPMC의 고유한 친수성이 흡수력 향상에 결정적으로 작용했음을 시사한다.
5. In vitro 세포독성 분석 결과, SHNFs는 low control과 통계적으로 유의한 차이를 보이지 않았으며, high control에 비해 LDH 방출 수치가 뚜렷하게 낮았다. NIH 3T3 세포에 대한 세포독성 반응은 유도되지 않았으며, SHNFs는 생물학적 무해성과 우수한 세포친화성을 지닌 것으로 판단된다.
6.종합적으로, SHNF1은 섬유 균일성, 공정 안정성, 기계적 성능, 수분 흡수력 및 생체적합성 측면에서 균형 잡힌 조성으로 판단되며, HPMC의 최적 함량은 1% (w/v)로 제안된다.
본 연구를 통해 확보된 SHNFs는 고습윤·고흡수 특성과 생물학적 무해성을 기반으로 하여, 창상 피복재뿐 아니라 다양한 조직재생 응용 분야에서도 활용 가능성이 기대된다.
감사의 글
이 논문은 2023년도 정부(산업통상자원부)의 재원으로 한국산업기술진흥원의 ‘바이오융복합기술 전문인력 양성사업’의 지원을 받아 수행된 연구임(No. P0017805).
References
- 1 F. V. Dos Santos, R. L. Siqueira, L. de Morais Ramos, S. A. Yoshioka, M. C. Branciforti, and D. S. Correa, "Silk Fibroin- derived Electrospun Materials for Biomedical Applications: A Review" , Int. J. Biol. Macromol., 2024, 254, 127641.custom:[[[-]]]
- 2 X. Zha, X. Xiong, C. Chen, Y. Li, L. Zhang, H. Xie, and Q. Jiang, "Usnic‐acid‐functionalized Silk Fibroin Composite Scaffolds for Cutaneous Wounds Healing" , Macromol. Biosci., 2021, 21, 2000361.custom:[[[-]]]
- 3 M. Mabrouk, H. H. Beherei, and D. B. Das, "Recent Progress in the Fabrication Techniques of 3D Scaffolds for Tissue Engineering" , Mater. Sci. Eng. C, 2020, 110, 110716.custom:[[[-]]]
- 4 G. H. Altman, F. Diaz, C. Jakuba, T. Calabro, R. L. Horan, J. Chen, H. Lu, J. Richmond, and D. L. Kaplan, "Silk-based Biomaterials" , Biomaterials, 2003, 24, 401−416.custom:[[[-]]]
- 5 X. Xu, Q. Sun, A. Xu, and X. Guo, "Biodegradable and Biocompatible Polyvinyl Alcohol/Silk Fibroin-Based Composite with Improved Strength" , J. Polym. Mater., 2022, 39, 167−181.custom:[[[-]]]
- 6 P. Heydari Foroushani, E. Rahmani, I. Alemzadeh, M. Vossoughi, M. Pourmadadi, A. Rahdar, and A. M. Díez- Pascual, "Curcumin Sustained Release with a Hybrid Chitosan-silk Fibroin Nanofiber Containing Silver Nanoparticles as a Novel Highly Efficient Antibacterial Wound Dressing", Nanomaterials, 2022, 12, 3426.custom:[[[-]]]
- 7 T. J. Sill and H. A. Von Recum, "Electrospinning: Applications in Drug Delivery and Tissue Engineering" , Biomaterials, 2008, 29, 1989−2006.custom:[[[-]]]
- 8 N. Bhardwaj and S. C. Kundu, "Electrospinning: A Fascinating Fiber Fabrication Technique" , Biotechnol. Adv., 2010, 28, 325− 347.custom:[[[-]]]
- 9 S. Thenmozhi, N. Dharmaraj, K. Kadirvelu, and H. Y. Kim, "Electrospun Nanofibers: New Generation Materials for Advanced Applications" , Mater. Sci. Eng. B, 2017, 217, 36−48.custom:[[[-]]]
- 10 C. M. Oh, P. W. S. Heng, and L. W. Chan, "A Study on the Impact of Hydroxypropyl Methylcellulose on the Viscosity of PEG Melt Suspensions Using Surface Plots and Principal Component Analysis", AAPS PharmSciTech, 2015, 16, 466− 477.custom:[[[-]]]
- 11 L. S. C. Wan, P. W. S. Heng, and L. F. Wong, "The Effect of Hydroxypropylmethylcellulose on Water Penetration into a Matrix System" , Int. J. Pharm., 1991, 73, 111−116.custom:[[[-]]]
- 12 F. Zhang, B. Zuo, Z. Fan, Z. Xie, Q. Lu, X. Zhang, and D. L. Kaplan, "Mechanisms and Control of Silk-based Electro- spinning" , Biomacromolecules, 2012, 13, 798−804.custom:[[[-]]]
- 13 I. H. Suhaime, M. Tripathy, and A. B. A. Majeed, "Sol-gel Transitions of Carbopol by Conductometric Investigation: The Impact of Hydroxypropyl Methylcellulose and Benzalkonium Chloride" , J. Chem. Pharm. Res., 2014, 6, 677− 687.custom:[[[-]]]
- 14 S. C. Joshi, "Sol-gel Behavior of Hydroxypropyl Methylcellulose (HPMC) in Ionic Media Including Drug Release" , Materials, 2011, 4, 1861−1905.custom:[[[-]]]
- 15 J. Y . Park and I. H. Lee, "Effect of Solvents on the Structure of Electrospun PVP Fiber" , J. Korean Ind. Eng. Chem., 2008, 19, 484−490.custom:[[[-]]]
- 16 H. J. Lee, T. M. Hong, S. C. Lim, J. S. Won, and S. G. Lee, "Preparation and Characterization of PVDF/PU Bicomponent Nanofiber by Electrospinning" , T ext. Sci. Eng., 2015, 52, 88−96.custom:[[[-]]]
- 17 D. Li and Y. Xia, "Electrospinning of Nanofibers: Reinventing the Wheel?" , Adv. Mater., 2004, 16, 1151−1170.custom:[[[-]]]
- 18 Y.-M. Lim, H.-J. Gwon, J. P . Jeun, and Y.-C. Nho, Preparation of Cellulose-based Nanofibers Using Electrospinning", Nanofibers, 2010, 179−188.custom:[[[-]]]
- 19 S. Khosravimelal, M. Chizari, B. Farhadihosseinabadi, M. Moosazadeh Moghaddam, and M. Gholipourmalekabadi, "Fabrication and Characterization of an Antibacterial Chitosan/silk Fibroin Electrospun Nanofiber Loaded with a Cationic Peptide for Wound-dressing Application", J. Mater. Sci. Mater. Med., 2021, 32, 114.custom:[[[-]]]
- 20 H. Zhang, L. Li, F . Dai, H. Zhang, B. Ni, W . Zhou, X. Y ang, and Y. Wu, "Preparation and Characterization of Silk Fibroin as a Biomaterial with Potential for Drug Delivery" , J. Transl. Med., 2012, 10, 117.custom:[[[-]]]
- 21 N. Amiraliyan, M. Nouri, and M. Haghighat Kish, "Structural Characterization and Mechanical Properties of Electrospun Silk Fibroin Nanofiber Mats" , Polym. Sci. Ser. A, 2010, 52, 407− 412.custom:[[[-]]]
- 22 A. D. Mali and R. S. Bathe, "Development and Evaluation of Gastroretentive Floating Tablets of a Quinapril HCl by Direct Compression Technique" , Int. J. Pharm. Pharm. Sci., 2017, 9, 35−46.custom:[[[-]]]
- 23 X. Li, L. Liu, H. B. Schlegel, "On the Physical Origin of Blue- shifted Hydrogen Bonds" , J. Am. Chem. Soc., 2002, 124, 9639− 9647.custom:[[[-]]]
- 24 M. Jahani, A. Asefnejad, M. H. Al-Musawi, A. A. Mohammed, B. T. Al-Sudani, M. H. Al-bahrani, N. A. Kadhim, M. Shahriari-Khalaji, H. Valizadeh, F. Sharifianjazi, M. Mehrjoo, K. Tavamaishvili, and M. Tavakoli, " Antibacterial and Wound Healing Stimulant Nanofibrous Dressing Consisting of Soluplus and Soy Protein Isolate Loaded with Mupirocin" , Sci. Rep., 2024, 14, 26397.custom:[[[-]]]