한주연 , 손예진 , 김주현 , 서원 , 송영석
인공수정체 응용을 위한 HEMA/PU 구조체
HEMA/PU Structures for Intraocular Lens Applications
Ju Yeon Han, Ye Jin Son, Ju Hyeon Kim, Won Seo, Young Seok Song
Abstract: Posterior capsular opacification (PCO) is a common complication after cataract surgery caused by the proliferation of residual lens epithelial cells. This study aimed to develop intraocular lenses (IOLs) with reduced PCO incidence by optimizing material composition and surface properties. Hydrophilic poly(2-hydroxyethyl methacrylate) (HEMA) was crosslinked with poly(ethylene glycol) diacrylate (PEGDA), and its thermal and optical properties were evaluated. The incorporation of PEGDA enhanced crystallinity and mechanical stability, particularly when a 15-minute solvent evaporation step was applied before curing. Furthermore, surface modification with a polyurethane (PU) coating increased hydrophobicity, which is expected to contribute to the suppression of PCO. The PU coating also preserved high optical transparency of over 90% at wavelengths above 400 nm and ensured appropriate stiffness, facilitating surgical handling. These results demonstrate that PEGDA crosslinking combined with PU surface coating improves the thermal stability, transparency, and mechanical integrity of the fabricated lenses. The approach applied in this study provides a practical framework for material design in intraocular lenses aimed at reducing posterior capsular opacification.
Keywords: intraocular lens (IOL) , posterior capsular opacification (PCO) , poly(2-hydroxyethyl
1. 서 론
백내장은 수정체 혼탁으로 시력을 저하시켜 인공수정체 (intraocular lens, IOL) 삽입을 통한 수술이 필요하다1]. 그러나 수술 후 후낭혼탁(posterior capsule opacification, PCO)은 남아 있는 렌즈상피세포(lens epithelial cell, LEC)가 증식하여 발생하는 가장 흔한 합병증으로, 심할 경우 레이저 후낭절개술이나 인공수정체 교체술이 요구된다[2].
인공수정체의 재료와 표면 특성은 후낭혼탁 발생에 직접적인 영향을 미친다[3,4]. 기존 PMMA나 실리콘 소재는 투명성과 가공성은 우수하나 후낭혼탁 발생률이 높았으며, 현재 임상에서 널리 쓰이는 아크릴계 인공수정체는 친수성과 소수성으로 구분된다[5,6]. 대표적 친수성 소재인 poly(2-hydroxyethyl methacrylate) (pHEMA)는 우수한 투명성과 생체적합성으로 안과용 하이드로젤에 활용되어 왔으나[7,8], 소수성 아크릴보다 후낭혼탁 발생률이 높다는 한계가 보고되었다[9].
소수성 아크릴의 후낭혼탁 억제 기전은 Linnola가 제안한 샌드위치 이론으로 설명할 수 있다. 이론에 따르면 소수성 표면은 fibronectin 등 세포외기질 단백질의 흡착을 촉진하여 인공수정체–렌즈상피세포–후방낭막의 삼층 구조를 형성하고, 이를 통해 렌즈상피세포의 이동과 증식을 억제해 후낭혼탁을 줄일 수 있다[10−13].
기존에 후낭혼탁 발생률을 줄이기 위해 플라즈마 처리, 나노패터닝 등의 다양한 표면 개질 기법이 연구되었으나 비용과 공정 복잡성의 문제가 있다[14]. 대안으로 Linnola가 제안한 샌드위치 이론을 기반하여 비용 및 공정 복잡성을 줄이고자 했다.
본 연구는 인공수정체에 소수성 표면 특성을 부여하기 위한 소재로 polyurethane (PU)에 주목하였다. PU는 기계적 강도, 생체적합성, 가공 용이성이 우수하여 다양한 의료 소재에 적용되고 있으며, 특히 hexamethylene diisocyanate (HDI) 기반 PU는 표면 소수성 조절에 유리하다[15,16]. 본 연구에서는 pHEMA 필름을 제조할 때 가교제 poly(ethylene glycol) diacrylate (PEGDA)를 첨가하여 함량 변화 및 광개 시제 TPO의 용매 잔존 여부에 따른 열적 특성을 확인하고, PEGDA 함량과 코팅 여부에 따른 광투과도 변화를 분석하였다. 또한 PEGDA 및 PU 코팅 농도에 따른 수분 손실 특성을 평가하였으며, PU 코팅 적용이 기계적 강성과 표면 소수성에 미치는 영향을 검토하였다. 이러한 특성 변화를 바탕으로 후낭혼탁 억제와의 연계 가능성을 논의하였고, 인공수정체 모형을 제작하여 실제 제작 가능성을 확인하였다.
2. 실 험
2.1. 시약 및 시료
인공수정체 제조: 2-Hydroxyethyl methacrylate (HEMA, 96%)는 대정화금(Korea)에서 구입하여 사용하였다. Poly(ethylene glycol) diacrylate (PEGDA)는 Sigma-Aldrich (Korea)의 평균 분자량 700을 가교제로 사용하였다. Diphenyl(2,4,6-trimethylbenzoyl)phosphine oxide (TPO, 97%)는 Sigma-Aldrich (Korea)에서 구입하여 사용하였다.
Polyurethane (PU) 코팅: Polyurethane diol solution은 Sigma-Aldrich의 평균 분자량 320의 88 wt% 수용액으로 구입하여 사용하였다. Hexamethylene diisocyanate (HDI) 또한 Sigma-Aldrich에서 구입하여 사용하였다.
2.2. 시편 제조
인공수정체 형태로의 적용 가능성을 확인하기 위하여 해프틱(haptic)을 포함한 전체 직경 11 mm, 광학부 직경 5 mm, 두께 1.5 mm의 인공수정체 모델을 설계하여 이를 바탕으로 실리콘 재질의 몰드를 제작하였다. 이 몰드에 HEMA와 PEGDA를 중량비 1:1, 2:1, 3:1로 혼합한 전구체 용액을 주입하였다. 각 용액에 용매로 용해시킨 광개시제 TPO를 첨가하고 상온에서 0분 또는 15분간 방치하여 용매 일부를 증발시킨 후, 자외선 조사 장비(UV-handy lamp, LAB24, Korea)를 사용하여 UV-A 파장(365 nm)에서 광경화를 진행하고 24시간 동안 실온 건조하였다. 표면 소수성 개질을 위하여 경화된 시료에 폴리우레탄(polyurethane, PU) 코팅을 적용하였다. PU 용액은 polyurethane diol과 HDI(hexamethylene diisocyanate)를 혼합하여 제조하였으며, 에탄올과의 중량비를 1:10 및 1:8로 조절하여 농도를 변화시켰다. 코팅은 딥코팅(dip-coating) 방식으로 수행하였으며, 상온에서 예비 건조 후 [TeX:] $$50-60^{\circ} \mathrm{C}$$의 오븐에서 열경화를 진행하였다.
본 연구에서는 기계적 및 광학적 물성 비교를 용이하게 하기 위하여 모든 실험에서 인공수정체 대신 필름형 시편을 제조하였다. 필름 시편은 표준화된 형태로 실험 변수를 최소화할 수 있으며, 조성 변화에 따른 재료 고유 물성 평가에 적합하다. 또한 인공수정체 모형을 병행 제작하여, 동일한 조성 및 공정 조건이 실제 렌즈 형태로 구현 가능함을 확인하였다. 필름 시편은 HEMA/PEGDA/TPO 혼합액을 평판에 캐스팅하여 동일한 경화 및 건조 과정을 거친 후, PU 코팅을 적용하여 각종 분석에 활용하였다.
2.3. 분 석
열적 특성 분석: PEGDA 함량 변화 및 용액 제조 후 상온 방치 시간에 따른 열적 특성은 시차주사열량계(DSC; DSC 4000, PerkinElmer, USA)를 사용하여 분석하였다. 분석은 질소 분위기에서 승온 속도 [TeX:] $$10^{\circ} \mathrm{C} / \mathrm{min}$$의 조건으로 수행하였으며, 온도 범위는 [TeX:] $$15-300^{\circ} \mathrm{C}$$로 설정하였다.
광투과 특성 분석: PEGDA 함량 변화와 PU 코팅 여부에 따른 광투과 특성을 확인하기 위하여 분광광도계 (Cary 60 UV-Vis, Agilent Technologies, USA)를 사용하였다. 측정은 300−700 nm 파장 범위에서 자외선-가시광선(UV-Vis) 분광법으로 측정하였다.
수분 손실 특성 분석: PEGDA 및 PU 코팅 농도에 따른 시편의 수분 손실 특성은 수분 손실률을 통해 비교 분석하였다. 조건별로 제조된 시편은 동일한 규격으로 준비한 후, 24시간 실온에서 탈이온수에 침지하였다. 표면수를 제거한 뒤 초기 무게[TeX:] $$\left(W_{\text {initial }}\right)$$를 측정하였으며, 이후 [TeX:] $$50^{\circ} \mathrm{C}$$에서 24시간 동안 건조한 후 건조 후 무게[TeX:] $$\left(\mathrm{W}_{\mathrm{dry}}\right)$$를 측정하였다. 모든 측정은 동일 조건에서 3회 반복하여 평균값으로 나타내었다. 수분 손실률은 다음 식을 이용하여 계산하였다:
표면 소수성 분석: PEGDA 및 PU 함량 변화에 따른 인공수정체 표면의 소수성 평가는 접촉각 분석 장비(Pheonix-300, Surface Electro Optics, Korea)를 사용하여 세실 드롭법(Sessile droplet method)으로 수행하였다. 시료 표면의 수분을 충분히 제거한 후, 슬라이드 글라스 위에 고정하고, 동일한 부피의 물방울을 떨어뜨려 수 mm초 이내에 3회 측정을 실시하여 평균값으로 나타내었다.
기계적 특성 분석: 기계적 특성 평가는 범용 인장 시험기 (Universal Testing Machine, UTM; Model 3365, Instron, USA)를 사용하여 수행하였다. ASTM D882 규격에 따라 기계 방향(machine direction, MD)으로 길이 400 mm, 너비 5 mm의 필름 형태로 절단하여 파지 거리 20 mm, 인장 속도 2 mm/min 조건으로 수행하였다. 각 조건은 3회 반복 측정을 통해 평균값으로 나타내었다.
3. 결과 및 고찰
3.1. 광 조사 전 용매 부분 증발 과정이 안정성에 주는 영향
Figure 1은 HEMA와 PEGDA의 혼합 비율에 따른 용매 증발 시간 차이로 인한 열적 특성을 DSC로 분석한 결과이다. (a)는 시료를 혼합 직후 용매 증발 과정 없이 바로 광경화한 시편이고, (b)는 동일 조성의 시료를 혼합한 후 상온에서 15분간 부분적으로 용매를 증발시킨 후 광경화를 거친 시편이다. (b)는 (a)에 비하여 흡열 피크의 온도가 전반적으로 상승하고 피크 면적 또한 증가하였다. 이러한 변화는 고분자 결정 영역이 보다 잘 보존되었음을 의미하며, 용매에 의한 탈결정화가 억제된 결과로 해석된다. Ferchichi 등[17]은 용매가 결정 영역에 침투하면 탈결정화가 일어나 DSC에서 녹는점[TeX:] $$\left(\mathrm{T}_{\mathrm{m}}\right)$$이 낮아지고, 융해 엔탈피[TeX:] $$(\Delta \mathrm{H})$$ 줄어든다고 보고하였다. 본 연구에서 관찰된 흡열 피크의 상승과 융해 엔탈피의 증가는 이러한 메커니즘과 맥락을 같이하며, 경화 전 부분적인 용매 증발 과정이 탈결정화를 억제하고 결과적으로 더 뚜렷하고 재현성 있는 열적 특성이 확보됨을 시사한다. 또한 PEGDA가 포함된 시료에서는 PEGDA 함량이 증가할수록 부분 용매 증발 후 융해 엔탈피가 뚜렷하게 증가하였으며, 이는 용매 제거 이후 경화 과정에서 PEGDA와 HEMA 간의 가교 결합이 보다 효율적으로 진행된 결과로 해석된다. 따라서 용매 증발 정도는 HEMA/PEGDA 구조체의 열적 특성을 좌우하는 중요한 변수임을 알 수 있다.
Figure 1.
3.2. PEGDA 함량 변화 및 PU 코팅에 따른 광투과율 변화
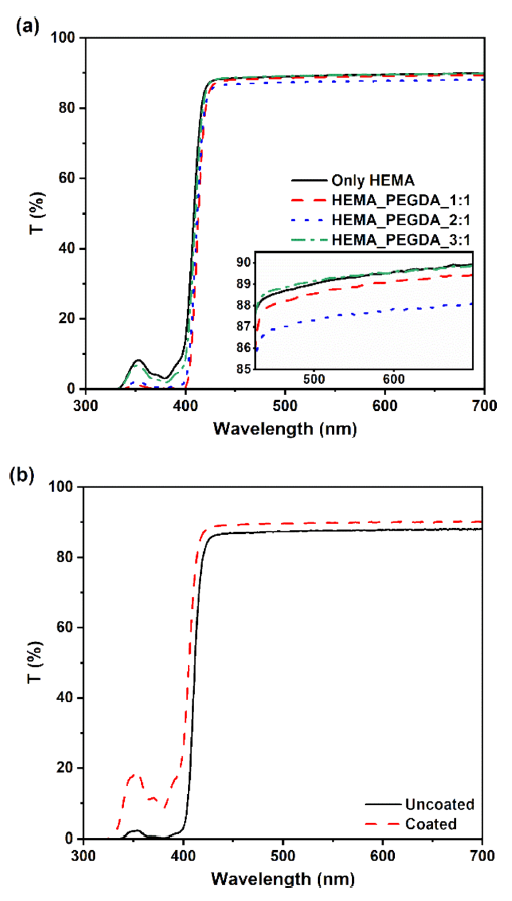
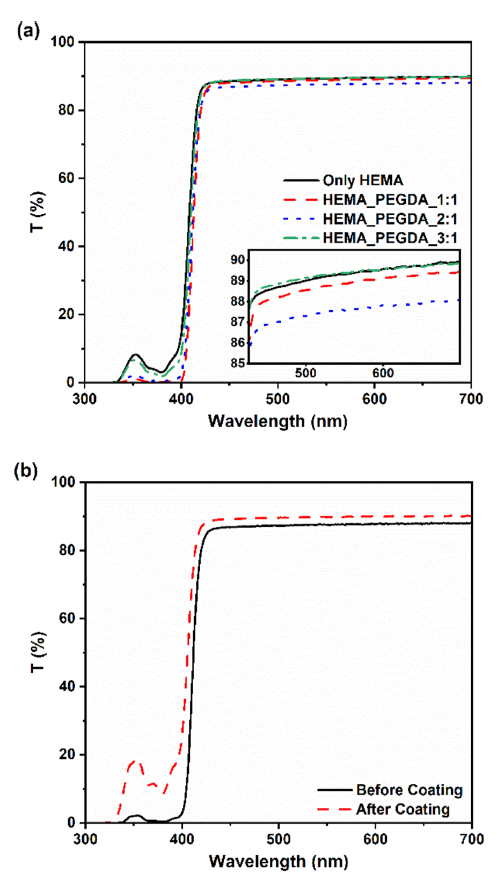
Figure 2는 300−700 nm 파장 범위에서의 UV-Vis 투과 스펙트럼이다. (a)는 코팅 전 HEMA에 대한 PEGDA 함량 변화에 따른 시편의 투과율을, (b)는 동일한 조성(HEMA: PEGDA=1:1) 시편을 PU로 코팅하기 전후의 투과율을 비교한 결과이다. (a)에서는 400 nm 이상의 파장 영역에서 모든 시편이 약 90%의 광투과율을 나타냈다. 이러한 이러한 투과율은 상용 인공수정체에서 보고된 스펙트럼 특성과 유사한 수준으로[18], 상용을 위한 광학적 적합성을 뒷받침한다. (b)에서는 PU 코팅된 시편이 전반적으로 코팅 이전보다 높은 투과율을 나타냈다. 광학적으로 총 산란(TIS)은 표면 거칠기 σ에 대해 [TeX:] $$\text { TIS } \propto(4 \pi \sigma / \lambda)^2$$로 증가하는 것으로 알려져 있으며[19], 동일 시편의 코팅 전·후에서 관찰된 투과율 증가는 표면 산란이 감소한 결과로 해석된다. 실제로 딥코팅 공정은 표면 레벨링을 통해 σ를 낮춰 투명도를 향상시키는 방법으로 보고된 바 있으며[20] 연구에서의 투과율 향상 역시 이러한 표면 평탄화 효과와 관련됨을 시사한다.
Figure 2.
3.3. PU 용액 농도에 따른 수분 손실률의 영향
Figure 3과 Table 1은 HEMA:PEGDA 비율(1:1, 2:1, 3:1) 및 PU:에탄올 조건(1:10, 1:8)에 따른 시편의 수분 손실률을 비교한 결과이다. 전반적으로 PU 코팅된 시편은 무코팅 대비 손실률이 낮았으며, HEMA 비율이 높을수록 억제 효과가 뚜렷하였다. 또한 코팅 조건에서는 표준편차가 줄어들어 보다 안정적인 거동을 보였으며, 정량적 수치는 Table 1에 제시하였다.
Figure 3.
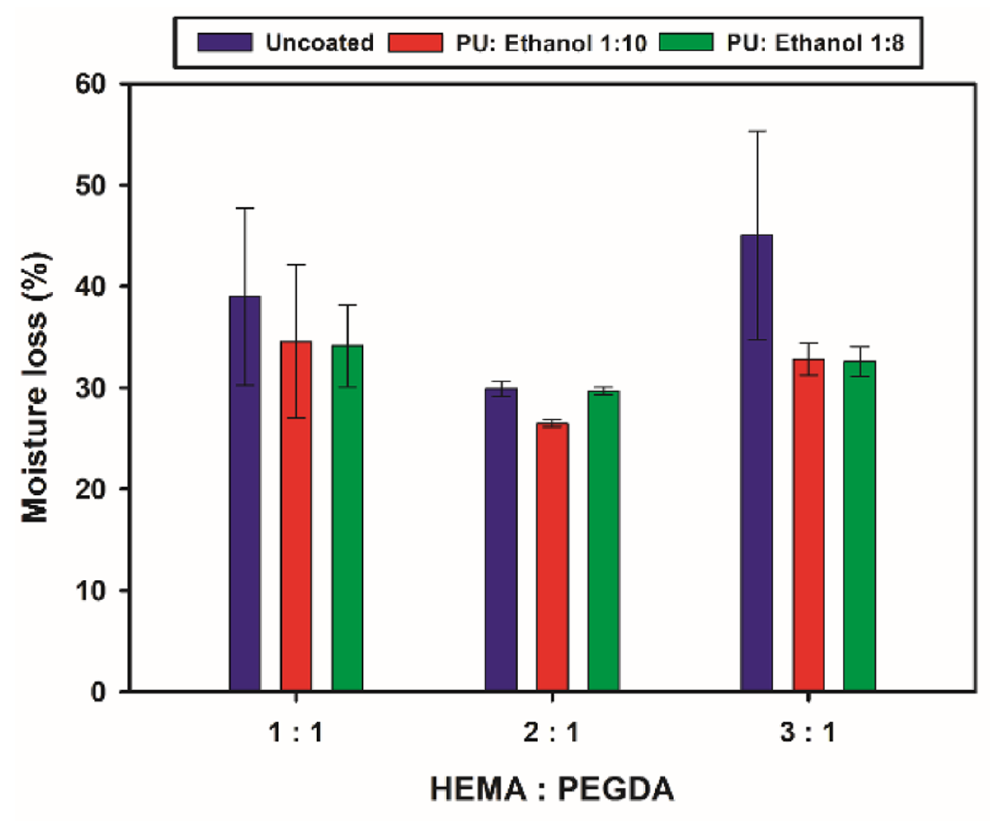
Table 1.
| HEMA:PEGDA ratio | PU:EtOH ratio | Moisture loss (%) (mean ± SD) |
|---|---|---|
| 1:1 | - | 36.98 ± 8.75 |
| 1:10 | 34.56 ± 7.57 | |
| 1:8 | 34.16 ± 4.07 | |
| 2:1 | - | 29.91 ± 0.73 |
| 1:10 | 26.48 ± 0.34 | |
| 1:8 | 29.70 ± 0.36 | |
| 3:1 | - | 45.05 ± 10.29 |
| 1:10 | 32.85 ± 1.59 | |
| 1:8 | 32.60 ± 1.45 |
3.4. 기계적 특성 평가
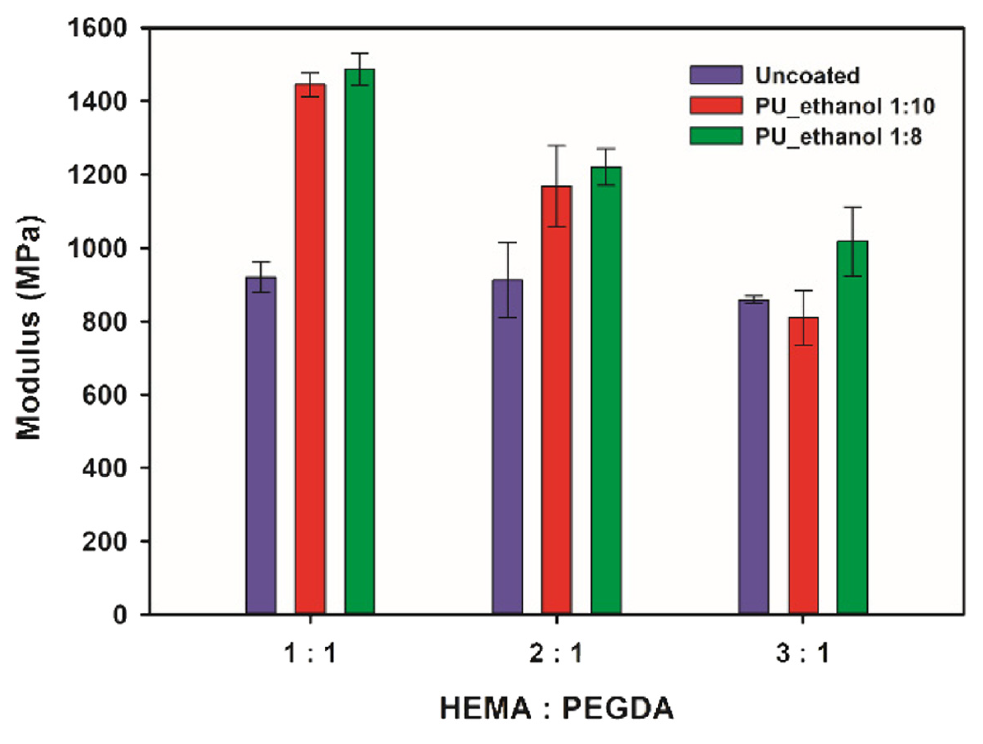
Figure 4는 비코팅 시편과 PU:에탄올 비율을 각각 1:10 및 1:8로 조절하여 코팅한 시편의 Young’s modulus를 비교한 결과이다. 본 연구에서 인공수정체 재료의 기계적 특성을 평가하기 위해 modulus를 주요 지표로 삼았다. modulus는 수술 과정에서 충분한 유연성을 확보하면서도 광학적 안정성을 유지하는 데 핵심적이다. Young’s modulus가 지나치게 크면 삽입 시 인공수정체를 펼치는 것이 어려울 수 있고[21], 반대로 너무 작으면 안구 내 위치 안정성 및 형태 유지에 불리할 수 있다. modulus는 이와 같은 안구 내에서의 거동을 예측할 수 있는 지표가 될 수 있다. 코팅된 시편은 비코팅 시편에 비해 전반적으로 modulus가 증가하였고, 이는 PU 코팅이 기계적 강성에 영향을 준다고 볼 수 있다. PU 코팅층이 추가적인 보강층 역할을 하여 표면에서의 응력 전달을 강화한 것으로 해석된다. 또한 HEMA 함량이 증가할수록 가교 밀도가 낮아져 modulus가 감소하는 경향을 보였다. 코팅된 시편에서 PU:에탄올 비율이 1:8 경우가 1:10인 경우보다 더 높은 modulus를 보였으며, 이는 PU 농도가 재료의 강성에 영향을 주는 요인임을 보여준다.
3.5. PEGDA 함량 변화 및 PU 코팅에 따른 표면 접촉각 변화
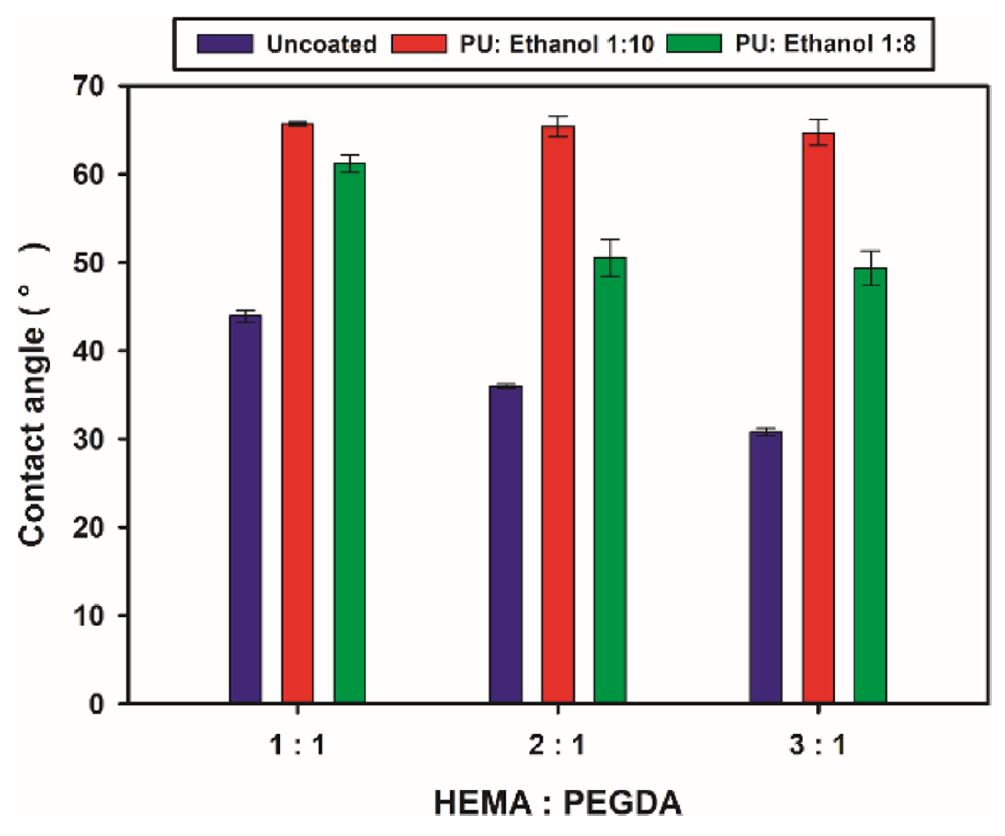
Figure 5는 HEMA와 PEGDA의 조성비(1:1, 2:1, 3:1)에 따른 비코팅 시편과 PU:에탄올 (1:10, 1:8) 조건으로 코팅한 시편의 접촉각 변화를 나타낸 것이다. PU 코팅된 시편은 비코팅 대비 접촉각이 전반적으로 높았으며, 이는 PU 코팅 시에 소수성이 부여되는 결과로 해석된다. 특히 PU:에탄올 1:10일 때, 상대적으로 큰 상승이 관찰되었다. 이는 코팅 농도가 낮을수록 표면에 더 높은 소수성을 부여할 수 있다. 한편 HEMA 함량이 증가할수록 접촉각은 감소하였으며, 이는 친수성 HEMA 함량이 증가할수록 코팅 효과가 상대적으로 약화된 결과로 이해된다. 이러한 경향은 후낭혼탁 억제와의 연계 가능성을 시사한다. 관찰된 접촉각 상승은 표면 소수성 증가를 반영하며, Linnola 등이 제시한 샌드위치 이론(Sandwich theory)[10−13]에 기반하여 소수성 표면은 세포외기질 단백질의 흡착을 촉진하고, 이를 통해 흡착된 단백질은 렌즈상피세포(LEC)의 단층 부착을 매개하여 인공수정체–세포 단층–후방낭막의 삼층 구조를 형성한다. 이 구조는 세포의 광학부 하방 이동을 차단하고, 이미 부착된 세포의 증식 및 분화를 지연시켜 후낭혼탁 발생을 억제하는 기전으로 설명될 수 있다.
3.6. HEMA-PEGDA/PU 인공수정체의 설계 구현
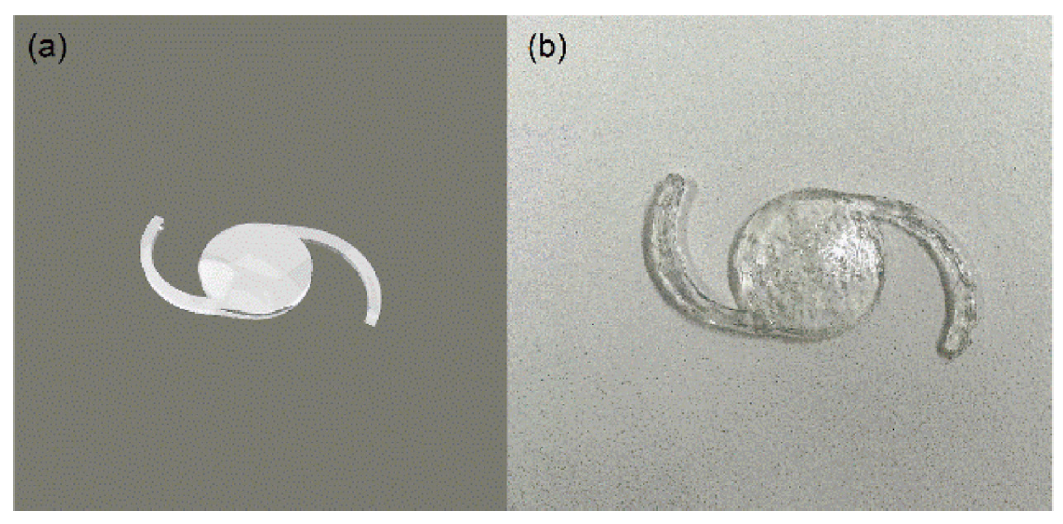
Figure 6은 (a)설계된 인공수정체의 3D CAD 모델과 이를 (b)실제로 제작한 모형을 비교한 결과이다. 전체 형상과 중심 광학부는 안정적으로 구현되었으며, 제작 과정에서 발생한 표면 요철은 PU 코팅을 통해 완화되었다. 또한 코팅은 소수성 및 항세포접착 기능 확보에도 긍정적으로 작용할 것으로 기대된다.
4. 결 론
본 연구에서는 HEMA-PEGDA 기반 소재와 PU 표면 코팅 공정을 적용하여 인공수정체의 물리적·광학적 성능을 확보 및 후낭혼탁(PCO) 억제 가능성을 제시하였다. 실제 제작한 인공수정체는 형상 안정성과 재현성 및 높은 광투과율을 보였다. 또한 PU 코팅은 투명성 저하 없이 소수성을 향상시키고, 수분 손실을 억제하여 표면 특성을 개선하였으며, 접촉각 상승과 표면 소수성 향상 결과를 근거로 세포 부착 억제 가능성을 추론하였다. 따라서 본 연구는 세포 실험을 통한 직접적 검증 이전 단계에서 여러 실험을 통해 적용 가능성을 검토하여 후낭혼탁 예방을 위한 소재 설계의 타당성을 입증하였다.
References
- 1 I. M. Wormstone, "Posterior Capsule Opacification: A Cell Biological Perspective" , Exp. Eye Res., 2002, 74, 337-347.custom:[[[-]]]
- 2 I. M. Wormstone, L. Wang, and C. S. C. Liu, "Posterior Capsule Opacification" , Exp. Eye Res., 2009, 88, 257-269.custom:[[[-]]]
- 3 W . Buehl and O. Findl, "Effect of Intraocular Lens Design on Posterior Capsule Opacification", J. Cataract Refract. Surg., 2008, 34, 1976-1985.custom:[[[-]]]
- 4 C. Luo, Q. Yuan, Y. Zhang, J. Xiao, Y. Huang, and Y. Yang, "Recent Advances of Intraocular Lens Materials and Surface Modification in Cataract Surgery" , Front. Bioeng. Biotechnol., 2022, 10, 913383.custom:[[[-]]]
- 5 M. J. Kim, H. Y. Lee, and C. K. Joo, "Development of After- cataract in Pseudophakic Eyes with Silicone or PMMA Intraocular Lens. " , J. Korean Ophthalmol. Soc., 1998, 39, 2653- 2660.custom:[[[-]]]
- 6 R. J. Olson, N. Mamalis, L. Werner, and D. J. Apple, "Cataract Treatment in the Beginning of the 21st Century", Am. J. Ophthalmol., 2003, 136, 146-154.custom:[[[-]]]
- 7 H. Wu, J. Y ang, Z. Wang, Y . Liu, X. Hu, and X. Huang, "Eye of the future: Unlocking the Potential Utilization of Hydrogels in Intraocular Lenses" , Bioeng. Transl. Med., 2024, 9, e10664.custom:[[[-]]]
- 8 M. Zare, H. R. Ramezani, S. A. Motahari, and M. Ghasemi, "pHEMA: An Overview for Biomedical Applications", Int. J. Mol. Sci., 2021, 22, 6376.custom:[[[-]]]
- 9 A. Grzybowski, R. Zemaitiene, A. Markeviciute, and R. Tuuminen, "Should we Abandon Hydrophilic Intraocular Lenses?" , Am. J. Ophthalmol., 2022, 237, 139-145.custom:[[[-]]]
- 10 R. J. Linnola, "Sandwich Theory: Bioactivity-based Explanation for Posterior Capsule Opacification" , J. Cataract Refract. Surg., 1997, 23, 1539-1542. Figure 5. Contact angles of the uncoated and polyurethane-coated samples. Figure 6. (a) Schematic 3D model of the IOL and (b) photograph of the 3-D printed IOL model.custom:[[[-]]]
- 11 R. J. Linnola and A. Holst, "Evaluation of a 3-piece Silicone Intraocular Lens with Poly(methyl methacrylate) Haptics", J. Cataract Refract. Surg., 1998, 24, 1509-1514.custom:[[[-]]]
- 12 R. J. Linnola, L. Werner, S. K. Pandey, M. Escobar-Gomez, S. L. Znoiko, and D. J. Apple, "Adhesion of Fibronectin, Vitronectin, Laminin, and Collagen Type IV to Intraocular Lens Materials in Pseudophakic Human Autopsy Eyes: Part 1: Histological Sections", J. Cataract Refract. Surg., 2000, 26, 1792-1806.custom:[[[-]]]
- 13 R. J. Linnola, L. Werner, S. K. Pandey, M. Escobar-Gomez, S. L. Znoiko, and D. J. Apple, "Adhesion of Fibronectin, Vitronectin, Laminin, and Collagen Type IV to Intraocular Lens Materials in Pseudophakic Human Autopsy Eyes: Part 2: Explanted Intraocular Lenses" , J. Cataract Refract. Surg., 2000, 26, 1807-1818.custom:[[[-]]]
- 14 Y . C. Cho and J. M. Park, "Delayed Opacification of Hydrophilic Acrylic IOLs with Hydrophobic Surface after Vitrectomy", J. Korean Ophthalmol. Soc., 2020, 61, 1225-1229.custom:[[[-]]]
- 15 J. Joseph, R. M. Patel, A. W enham, and J. R. Smith, "Biomedical Applications of Polyurethane Materials and Coatings" , Mater. Sci. Technol., 2018, 34, 121-129.custom:[[[-]]]
- 16 V . L. Covolan, L. C. Oliveira, A. G. Ferreira, A. C. Leite, and R. B. Costa, "Polyurethane-based Materials for the Production of Biomedical Materials" , Macromol. Symp., 2004, 218, 273−282.custom:[[[-]]]
- 17 S. Ferchichi, F. Collas, O. Boyron, M. Rey-Bayle, V. Monteil, and N. Sheibat-Othman, "Differential Scanning Calorimetry for Characterizing Solvent-induced Decrystallization and Recrystallization of Polyolefins: Combination with in situ Raman Spectroscopy", Macromol. Chem. Phys., 2025, 226, e00088.custom:[[[-]]]
- 18 M. A. Mainster, "Violet and Blue Light Blocking Intraocular Lenses: Photoprotection Versus Photoreception", Br. J. Ophthalmol., 2006, 90, 784-792.custom:[[[-]]]
- 19 H. E. Bennett and J. O. Porteus, "Relation between Surface Roughness and Specular Reflectance at Normal Incidence" , J. Opt. Soc. Am., 1961, 51, 123-129.custom:[[[-]]]
- 20 A. Shrotri, S. Preu, and O. Stübbe, "Achieving Transparency and Minimizing Losses of Rough Additively Manufactured Optical Components by a Dip-coating Surface Finish", Coatings, 2025, 15, 210.custom:[[[-]]]
- 21 K. Ehrmann, E. Kim, and J. M. Parel, "Mechanical Properties of Intra-ocular Lenses" , Biomaterials, 2008, 29, 1582-1590.custom:[[[-]]]